ARTICOLO 2: PROGRESSI NEL CALCESTRUZZO PRECONFEZIONATO
1.0 Introduzione
Il calcestruzzo preconfezionato (1,2) è incentrato su tre attrezzature particolari:
- il premiscelatore;
- l’autobetoniera;
- la pompa.
1.1 Il Premiscelatore
Il premiscelatore (Fig.1.1), che è situato nella centrale di betonaggio, ha la funzione di mescolare a umido gli ingredienti prima che siano introdotti in autobetoniera con l’obiettivo di ottenere un impasto ben amalgamato, uniforme, privo di segregazione e bleeding ancorché fluido come un calcestruzzo autocompattante. Inoltre, questo calcestruzzo è più prestazionale del corrispondente calcestruzzo fresco mescolato introducendo gli ingredienti direttamente in autobetoniera.
Un calcestruzzo preconfezionato dotato di premiscelatore presenta due vantaggi:
- minore dispersione nella lavorabilità da un impasto all’altro nominalmente della stessa composizione;
- maggiore resistenza meccanica a compressione sia alle brevi che alle lunghe stagionature con possibilità di ammortizzare il costo di investimento del premiscelatore con un dosaggio di cemento leggermente inferiore (10%) per raggiungere la stessa prestazione conseguita mescolando il calcestruzzo direttamente in autobetoniera.

Fig. 1.1 – Vista di un edificio entro il quale è allocato il premiscelatore mentre alimenta due autobetoniere
1.2 L’autobetoniera
L’autobetoniera (Fig.1.2) è un carro mobile attrezzato con un contenitore (noto come “botte”) di una capacità di circa 10 m3 per il trasporto del calcestruzzo fresco dalla centrale di betonaggio al cantiere. Durante il tragitto la “botte” ruota lentamente per evitare la segregazione del calcestruzzo.
In molti impianti, purtroppo, il premiscelatore è assente e gli ingredienti sono introdotti direttamente in autobetoniera dove sono miscelati ad alta velocità: la costanza e le prestazioni del calcestruzzo sono molto inferiori rispetto a quelle conseguite se gli ingredienti sono introdotti a umido dopo averli mescolati ad alta velocità in un premiscelatore (§ 1.1).

Fig.1.2-Vista di un’autobetoniera
Dall’autobetoniera il calcestruzzo alimenta il sito da costruire in due modi:
- a) getto in caduta libera dall’autobetoniera al sito da costruire (Fig.1.3);
- b) getto mediante pompaggio in sito non raggiungibile dall’autobetoniera (Fig. 1.4).

Fig 1.3 Getto in caduta libera del calcestruzzo dall’autobetoniera
1.3 La pompa
La pompa è un elemento indispensabile quando dall’autobetoniera non è possibile gettare il calcestruzzo direttamente nel sito in costruzione. In questo caso è necessario che l’autobetoniera sia collegata con il sito dove occorre gettare il calcestruzzo mediante una pompa. La Fig.1.4 mostra il getto mediante pompaggio in un sito inaccessibile all’autobetoniera.

Fig. 1.4-Getto mediante pompaggio in sito non raggiungibile dall’autobetoniera (per gentile concessione di Heidelberg Materials Calcestruzzi)
1.4 Evoluzione del calcestruzzo preconfezionato
Secondo alcune fonti il primo impianto di calcestruzzo preconfezionato fu costruito nel 1913 in USA a Baltimora. Nel 1929 c’erano oltre 100 impianti che operavano in USA.
L’industria del calcestruzzo preconfezionato non si espanse significativamente fino agli anni 1960, e crebbe significativamente solo da allora. In Italia il calcestruzzo preconfezionato fu introdotto dall’imprenditore Ferruzzi di Ravenna con il nome di Calcestruzzi Spa alla fine degli anni 1950 e fu ceduta al gruppo Italcementi nel 1997. Oggi esistono cica 400 impianti di calcestruzzo preconfezionato prodotto da società associate all’ATECAP (Tabella 1).
Tabella 1 Impianti di calcestruzzo preconfezionato di società iscritte all’ATECAP*
| RAGIONE SOCIALE | IMPIANTI |
| A.CE.MA.T. S.R.L. | 1 |
| BASTIAN CALCESTRUZZI S.R.L. | 1 |
| BETON LANA S.R.L. | 1 |
| BETONCAVE S.R.L. | 1 |
| BETONCIFALDI S.R.L. | 1 |
| BETONFAS S.R.L. | 1 |
| BETONROSSI S.P.A. | 35 |
| BIESSE 2000 S.R.L. | 1 |
| BLANCO ORAZIO CALCESTRUZZI S.R.L. | 1 |
| CALCESTRUZZI DELLA VAL ROJA S.R.L. | 1 |
| CALCESTRUZZI ERBESI S.R.L. | 1 |
| CALCESTRUZZI FIORENTINI S.R.L. | 9 |
| CALCESTRUZZI LARIO 80 S.P.A. (DELEGA) | 1 |
| CALCESTRUZZI S.P.A. | 102 |
| CAVA SAN BERNARDINO S.R.L. | 1 |
| CAVIR CALCESTRUZZI S.R.L. | 1 |
| COLABETON S.P.A. | 77 |
| CONGLOBIX S.N.C. | 1 |
| COOPERATIVA TRASPORTI IMOLA SCRL | 1 |
| CORONA CALCESTRUZZI S.R.L. | 1 |
| CONCRETE ITALIA SRL | 10 |
| CRUCITTI GROUP S.R.L. | 1 |
| EFFE 5 COSTRUZIONI S.R.L. | 1 |
| ES.CAL. S.R.L. | 1 |
| F.LLI CHERCHI S.R.L. | 1 |
| F.LLI DE PRA S.P.A. | 4 |
| FRATELLI MAZZA S.R.L. | 1 |
| FRIULANA CALCESTRUZZI S.P.A. | 5 |
| GRUPPO GATTI S.P.A. | 7 |
| GUIDO RUGGIU S.R.L. | 1 |
| HOLCIM AGGREGATI CALCESTRUZZI S.R.L. | 9 |
| I.C.E.A. S.R.L. DEI F.LLI DI FEDE | 1 |
| IMPRESA OLIVOTTO S.R.L. | 1 |
| IMPRESE PESENTI S.R.L. | 2 |
| INERTI E CALCESTRUZZI S.R.L. (DELEGA) | 1 |
| INERTI VALFINO S.R.L. | 1 |
| ITALCAVE S.R.L. | 1 |
| LA GARIGLIANO S.R.L. | 1 |
| LATINA BETON S.R.L. | 1 |
| LUCIANI S.P.A. (DELEGA) | 3 |
| LUIGI METELLI S.P.A. | 1 |
| MAGESTE SRL | 1 |
| MASSANO AURELIO CALCESTRUZZI S.R.L. | 1 |
| MASTERBETON S.R.L. | 1 |
| MAZZOCCO ROMOLO S.R.L. | 1 |
| OEMME CALCESTRUZZI S.R.L. | 1 |
| PANARESE CALCESTRUZZI S.A.S. | 1 |
| S.A.E.G.A. S.P.A. | 1 |
| S.A.I.S.E.F. S.P.A. | 1 |
| SALICE CALCESTRUZZI S.R.L. | 1 |
| STROPPIANA S.P.A. | 1 |
| SUPERBETON S.P.A. | 10 |
| TOMATIS GIACOMO S.R.L. | 1 |
| UNIBETON & SERVICES S.R.L. | 2 |
| UNICAL S.P.A. | 105 |
*Fonte ATECAP
Si stima che il calcestruzzo preconfezionato rappresenti circa l’80% della produzione totale in Italia. Nelle centrali di betonaggio si mescolano determinate quantità di ghiaia, sabbia, acqua e cemento in base alle proprietà richieste dal progettista.
Il calcestruzzo preconfezionato è spesso impiegato al posto di altri materiali per il minor costo specialmente in costruzioni di grandi dimensioni, come i ponti ed altre strutture socialmente importanti. Il calcestruzzo preconfezionato è impiegato dove la produzione del calcestruzzo non può avvenire in sito. L’’impiego del calcestruzzo preconfezionato comporta che il prodotto sia consegnato a richiesta in forma finita, nella quantità specifica e in accordo alle prestazioni stabilite.
Le prestazioni del calcestruzzo preconfezionato possono essere modificate mediante l’impiego di additivi chimici. L’impiego di additivi richiede una precisione nel loro dosaggio che comporta l’adozione di apparecchiature di laboratorio e di dosaggio nella centrale di betonaggio. Gli additivi possono essere impiegati per ridurre la richiesta di acqua di impasto, per inglobare microbolle d’aria al fine di incrementare la resistenza ai cicli di gelo-disgelo, o anche per produrre calcestruzzi autocompattanti (3).
Nel caso di un trasporto molto lungo tra la centrale di betonaggio e il sito dove gettare il calcestruzzo esiste il problema della perdita di lavorabilità soprattutto in climi caldi. In questi casi, si può ovviare a questo inconveniente impiegando il prodotto SLCA acronimo inglese di Slump Loss Controlling Agent (4).Nel caso di un trasporto nel traffico congestionato delle grandi città si può arrivare a posizionare la centrale di betonaggio accanto al sito dove si costruisce come è avvenuto nella costruzione del MAXXI a Roma (§ 1.0, Articolo 4).Questa scelta deve,però,essere economicamente avvalorata dal tempo impiegato nella esecuzione della costruzione che deve essere almeno 2-3 anni.
BIBLIOGRAFIA
(1) SHELLY COMPANY, “The Shelly Company, pp.1,17, (2014).
(2) ARTHUR MICHAEL, “Concrete”, pg. 2, (2004).
(3) MARIO COLLEPARDI, SILVIA COLLEPARDI, ROBERTO TROLI, “Il Nuovo Calcestruzzo”, Settima Edizione, Edizioni TREVISOSTAMPA, pp. 233, 259, (2022).
(4) MARIO COLLEPARDI, SILVIA COLLEPARDI, ROBERTO TROLI, “Il Nuovo Calcestruzzo”, Settima Edizione, Edizioni TREVISOSTAMPA, pg.254, (2022).
INFORMAZIONI SUGLI AUTORI DEGLI ARTICOLI
Mario Collepardi si è laureato in Chimica Industriale con il massimo dei voti nell’Università La Sapienza di Roma. Nel 2007 ad Atlanta (USA) è stato nominato Honorary Member of the American Concrete Institute. Nel 2017 a Bergamo è stato nominato Socio Onorario dell’AICAP. Dal 1969 al 2004 ha insegnato Scienza e Tecnologia dei Materiali nelle Facoltà di Ingegneria delle Università di Cagliari, di Roma La Sapienza, di Ancona oltre che al Politecnico di Milano. È autore di oltre 400 pubblicazioni e di una decina di libri sul calcestruzzo pubblicati in italiano, inglese, cinese e ceco. Nel 1997 a Roma il Consiglio delle Ricerche del Canada e l’American Concrete Institute hanno organizzato in suo onore il “MARIO COLLEPARDI SYMPOSIUM”.
Silvia Collepardi si è laureata a Padova in Ingegneria Civile ed è Amministratore della EN.CO di Villorba (TV) dove è anche direttrice del Laboratorio Ufficiale per le prove sui materiali da Costruzione. È autrice di numerosi articoli e di alcuni libri sul calcestruzzo pubblicati in italiano, inglese e cinese. Nel 2015 ad Ottawa (Canada) Silvia Collepardi ha ricevuto l’Award dall’American Concrete Institute per i “significativi e costanti contributi nella vasta area della tecnologia del calcestruzzo e per la certificazione dei materiali per il loro impiego nel calcestruzzo”.
Roberto Troli si è laureato ad Ancona in Ingegneria Civile con il massimo dei voti e lode. Roberto Troli ha lavorato nella EN.CO come Direttore Tecnico per la messa a punto di nuovi calcestruzzi e per l’assistenza tecnica in contestazioni legali. È autore di numerosi articoli e di alcuni libri sul calcestruzzo pubblicati in italiano, inglese e cinese. Nel 2009 a Siviglia (Spagna) ha ricevuto l’Award dall’American Concrete Institute per i suoi “notevoli contributi alla fondamentale conoscenza dei superfluidificanti ed al loro impiego nel calcestruzzo”. Dal 2021 Roberto Troli è Direttore Tecnologico della Betonrossi di Piacenza.
Prescrizioni del progettista in accordo ad un programma automatico
Articolo 1
PRESCRIZIONI DEL PROGETTISTA IN ACCORDO AD UN PROGRAMMA
AUTOMATICO
1.0 Il ruolo del progettista
Il progettista delle costruzioni in calcestruzzo armato deve emanare le prescrizioni di capitolato per il produttore di calcestruzzo e per l’impresa che lo mette in opera, come anche deve inoltrare le istruzioni per i controlli al Direttore dei Lavori. Tali obblighi rispondono a quanto prescritto nelle Norme Tecniche delle Costruzioni (NTC) emanate con DM 17/01/2018 (1) e relativa Circolare esplicativa N.7 del 21/01/2019 (2).
In assenza di queste prescrizioni le costruzioni mostrano segni di degrado nel giro di qualche anno e possono perfino collassare nel giro di un decennio.
Il metodo per emettere le prescrizioni descritto nel seguito è semplice, rapido e sicuro.
Esso procede in accordo ad un programma automatico noto come E&Q (acronimo inglese di Easy&Quick): si tratta di rispondere ad una serie di domande al termine delle quali il programma elabora immediatamente le prescrizioni per il produttore di calcestruzzo e l’impresa, come anche le raccomandazioni per il Direttore Lavori.
Il metodo si basa sulla correlazione, secondo le vigenti Norme Europee, esistente tra il rapporto a/c e le prestazioni del calcestruzzo quali la Rck, la resistenza a compressione alle brevi stagionature (1-3-7 giorni), la resistenza meccanica a flessione e trazione, l’impermeabilità all’acqua, la durabilità. Per poter adottare questo metodo, e rispondere correttamente alle varie domande, occorre conoscere la Norma Europea sui cementi EN 197/1 (3), la classe di consistenza in termini di abbassamento al cono di Abrams, o più brevemente slump, indicata al prospetto 3 della EN 206 (4), le proprietà meccaniche ed in particolare la Rck, il degrado del calcestruzzo provocato dall’ambiente (classe di esposizione), la durabilità (almeno 50 o 100 anni) delle strutture nelle varie classi di esposizioni secondo la Norma Europea EN 206 e la EN 1992-1-1- Eurocodice 2 (5). Tutti questi argomenti sono trattati nella Settima Edizione del libro “Il Nuovo Calcestruzzo” (6). Relativamente al valore minimo di copriferro da prescrivere ai fini della durabilità, il programma prende come riferimento il (cmin,dur) riportato nella Tabelle 4.4N e 4.5N dell’Eurocodice 2 in funzione della classe di esposizione per una vita utile di 50 anni (classe della struttura S5). Nel caso di 100 anni di vita utile, sempre secondo quanto indicato nell’Eurocodice 2, verranno aggiunti 10 mm rispetto al valore prescritto per i 50 anni. Inoltre, secondo le indicazioni dell’Eurocodice 2, oltre a tale valore (cmin,dur) il progettista dovrebbe definire anche un valore aggiuntivo di sicurezza (Δcdev) scelto pari a 10 mm, 5 mm o 0 mm in base all’accuratezza della verifica dei sistemi di distanziatori che egli ipotizza possa essere adottata. Quindi, complessivamente, il copriferro nominale (cnom) che deve essere specificato sui disegni di progetto è definito come cnom = cmin,dur + Δcdev. Per opere di particolare rilevanza strategica il valore di Δcdev dovrebbe essere scelto eguale a 10 mm.
Per ogni correlazione esiste un rapporto (a/c)i ed il programma sceglie in automatico il valore più basso –(a/c)min– in modo che tutti requisiti prestazionale siano soddisfatti come è mostrato più avanti nelle Figure 27 e 48.
Il metodo si basa su una serie di videate in ciascuna della quali si pone una domanda alla quale occorre rispondere: per esempio, la struttura è armata o precompressa? Nell’esempio di seguito illustrato si esamina una costruzione intitolata ”Grattacielo di Roma” dove un grattacielo di 60 piani, costruito con un unico calcestruzzo in tutti i suoi piani, poggia su una fondazione incassata nel terreno.
A causa della risalita del pericoloso gas radon (Articolo 7) occorre inserire una barriera anti-radon tra la fondazione ed il pavimento del primo piano per evitare l’inquinamento radioattivo oltre i valori ritenuti pericolosi per la salute umana: 300 Bq/m3 o 200 Bq/m3 a seconda che le costruzioni siano erette rispettivamente prima o dopo il 31 dicembre 2024.
In particolare, il calcestruzzo per il grattacielo viene pompato con uno slump di 10-15 cm mentre per la fondazione si impiega un calcestruzzo superfluido con uno slump di 22-24 cm. Pertanto, sono stati elaborati i dati sui due diversi calcestruzzi, che si trovano di seguito nella Prima parte: fondazioni e nella Seconda parte: il Grattacielo. Al termine delle risposte alle varie videate il programma elabora in automatico le prescrizioni di capitolato per il produttore di calcestruzzo (§ 2.1 e § 3.1) e per l’impresa che lo deve mettere in opera (§ 2.2 e § 3.2) come anche le raccomandazioni per il Direttore dei Lavori (§2.3 e § 3.3).
Prima parte: fondazioni
Fig. 1 – Il nome dell’opera è Grattacielo di Roma
Fig. 2 – Il nome della struttura è Fondazione
Fig. 3 – La fondazione è Armata
Fig. 4 – Si adotta il cemento d’altoforno CEM III (per il basso calore di idratazione) perché la fondazione è un getto massivo
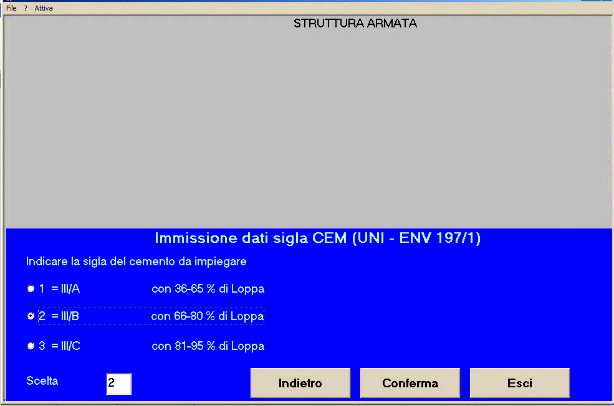
Fig. 5 – Il cemento da impiegare è di tipo III/B
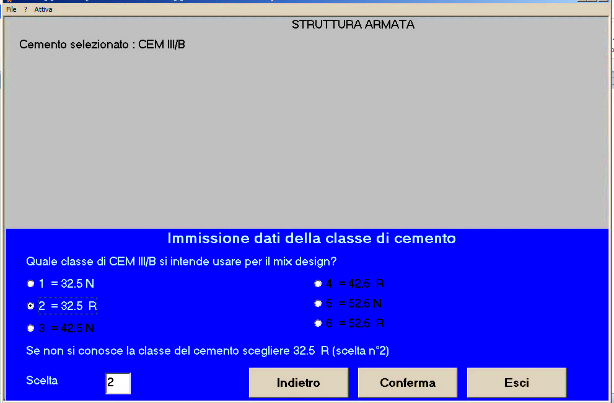
Fig. 6 – La classe di resistenza del cemento è 32.5 R
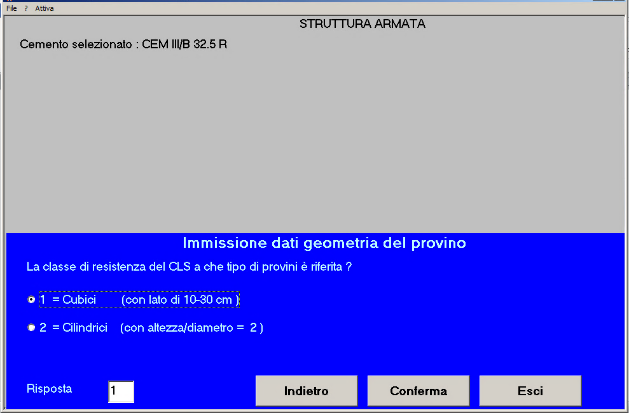
Fig. 7 – I provini per la misura della resistenza meccanica sono cubici
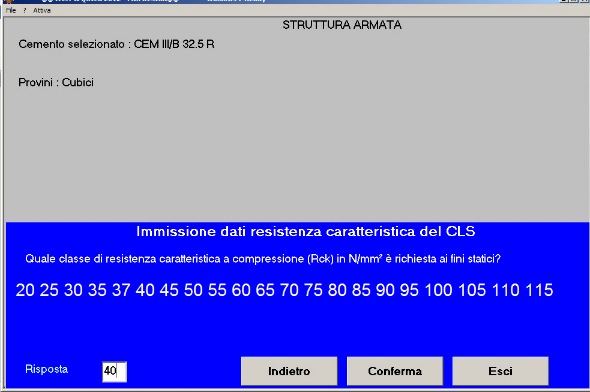
Fig. 8 – La Rck è 40 N/mm2
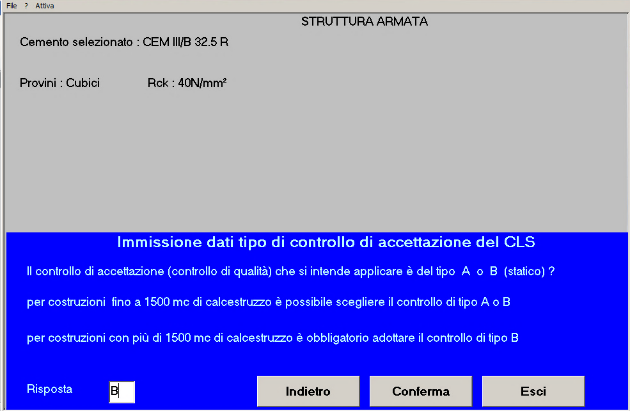
Fig. 9 – Il controllo è di tipo B
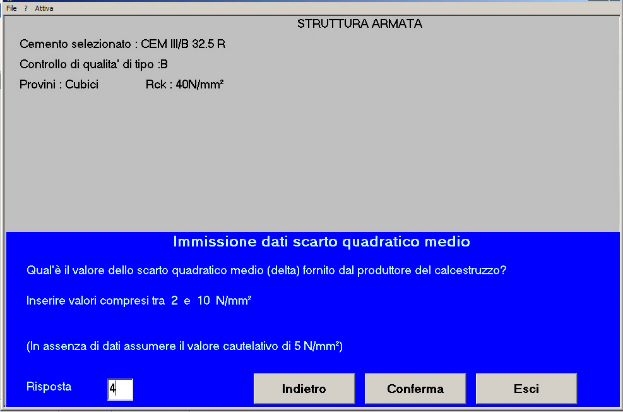
Fig. 10 – Lo scarto quadratico medio è 4 N/mm2
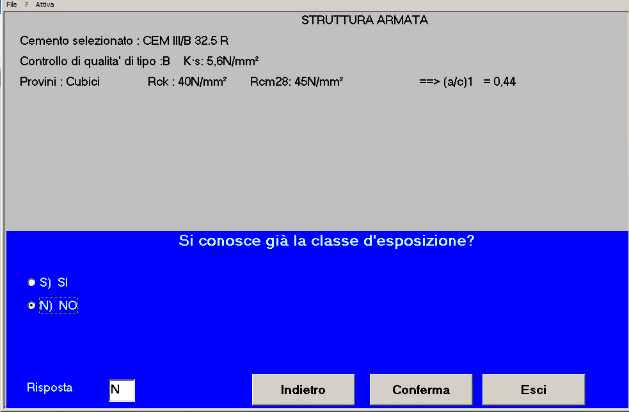
Fig.11 – Non si conosce la classe di esposizione
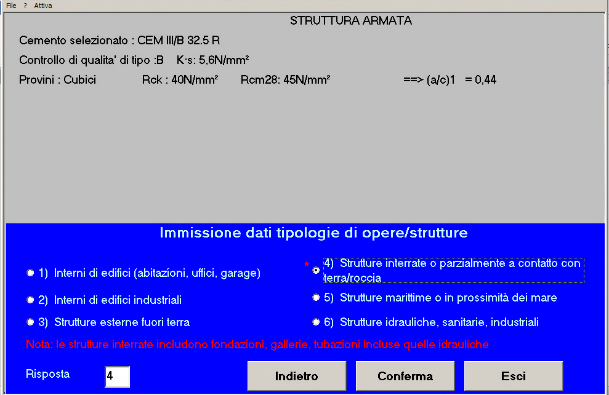
Fig. 12 – La struttura è interrata
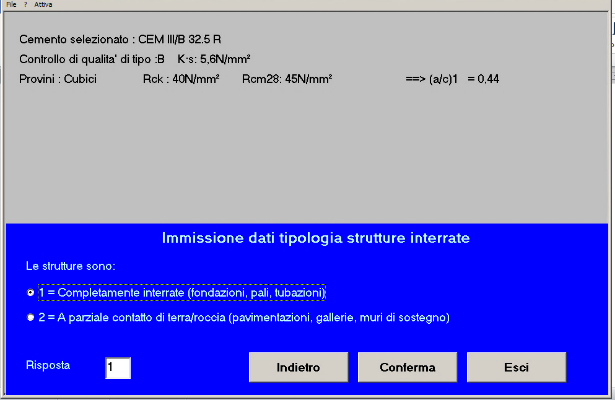
Fig. 13 – La struttura è completamente interrata
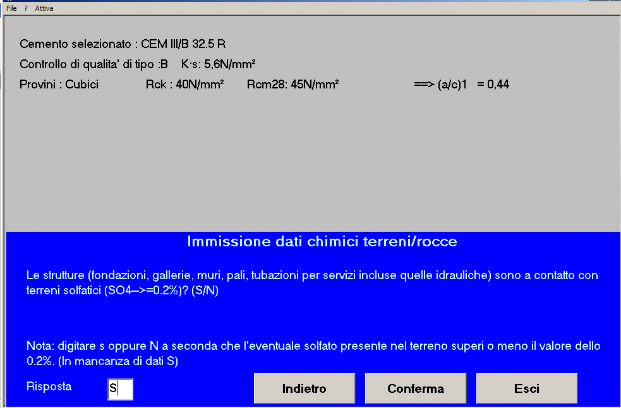
Fig.14 – La fondazione sarà a contatto con terreno solfatico
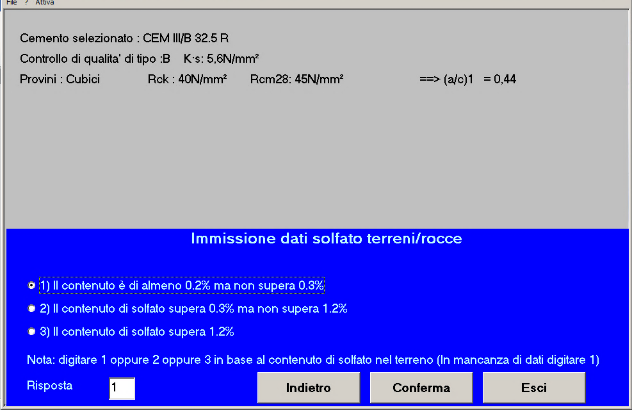
Fig. 15 – Il contenuto di solfato è compreso tra 0.2% e 0,3

Fig. 16 – Il terreno non è di natura acida
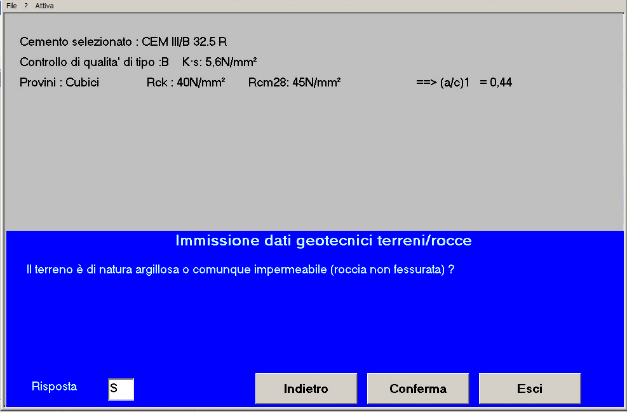
Fig. 17 – Il terreno è di natura argillosa
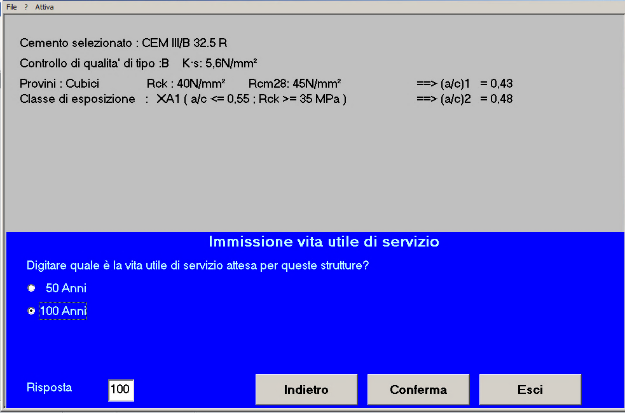
Fig.18 – La vita utile di servizio attesa è di almeno 100 anni
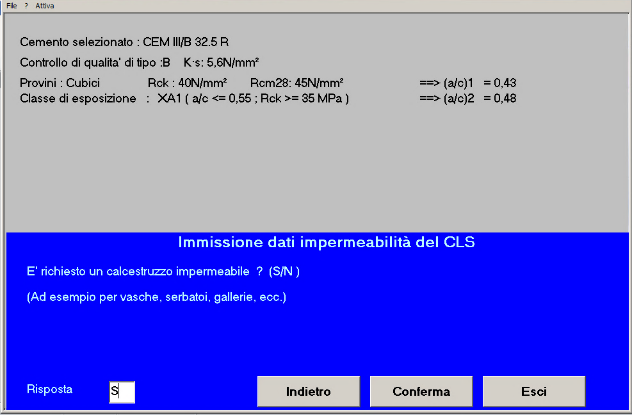
Fig. 19 – Si richiede un calcestruzzo impermeabile
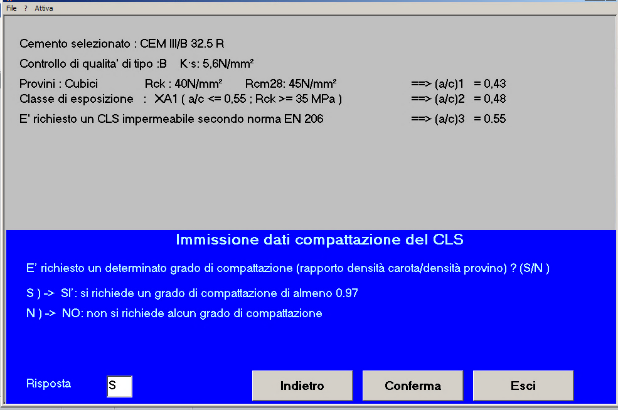
Fig. 20 – Il grado di compattazione richiesto è 0,97
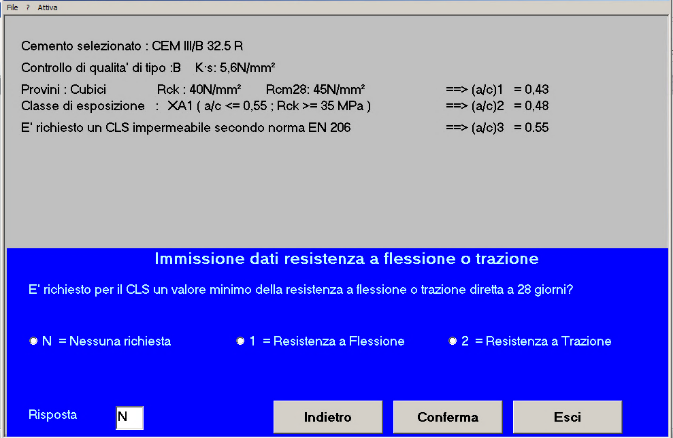
Fig. 21 – Non si richiede resistenza a flessione o a trazione
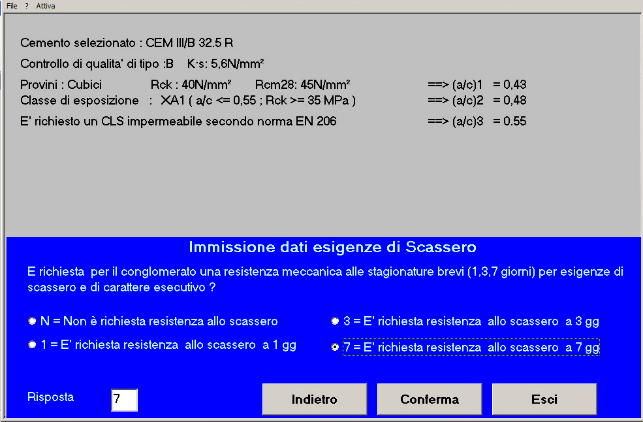
Fig. 22 – E’ richiesta una resistenza meccanica per lo scassero a 7 giorni
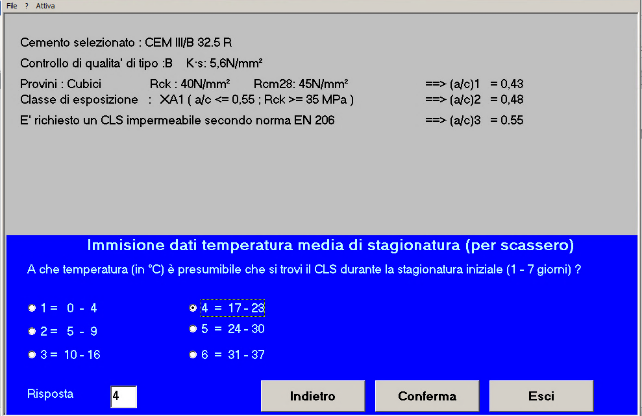
Fig. 23 – La temperatura presumibile nei primi 7 giorni sarà di 17-23°C
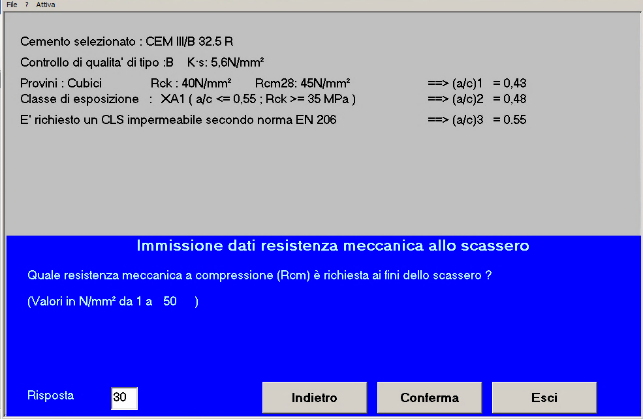
Fig. 24 – La resistenza meccanica a compressione richiesta a 7 giorni è 30 N/mm2
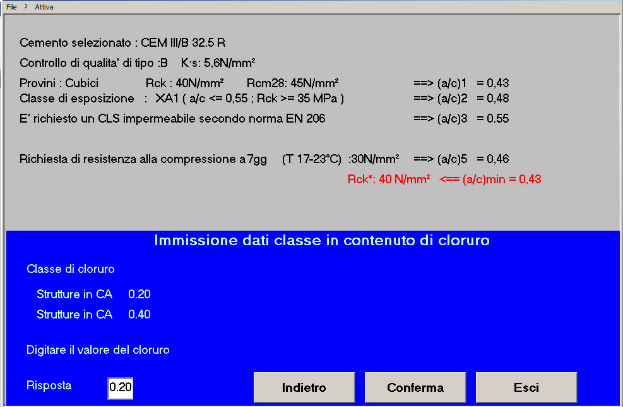
Fig. 25 – La classe di contenuto in cloruro è 0,20
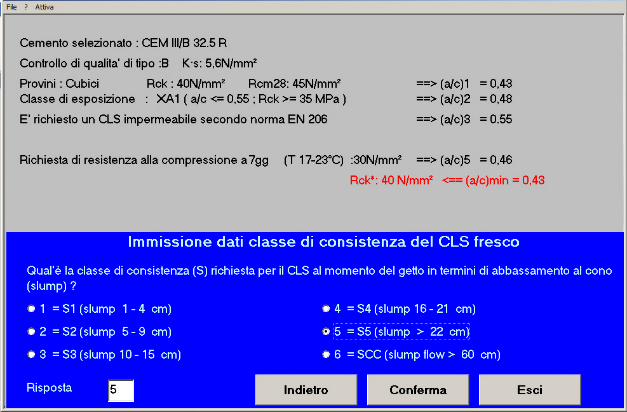
Fig. 26 – La classe di consistenza del calcestruzzo corrisponde ad uno slump > 22 cm
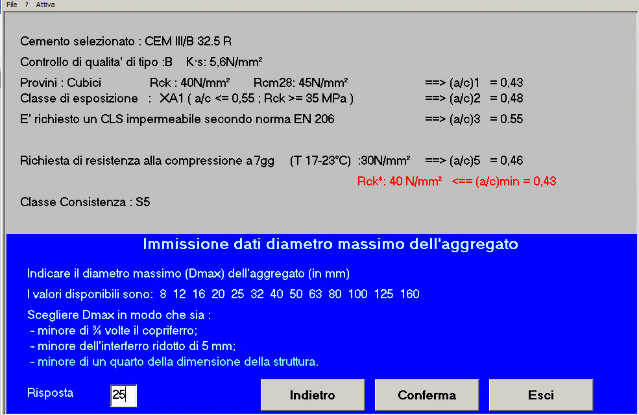
Fig. 27 – Il diametro massimo dell’aggregato è 25 mm
2 Prescrizioni di capitolato per la fondazione armata
Di seguito sono descritte le prescrizioni da inserire in capitolato per la Fondazione armata del Grattacielo di Roma con una durabilità di almeno 100 anni che riguardano il produttore di calcesruzzo e l’impresa che lo deve mettere in opera, come anche le raccomandazioni per il Direttore dei Lavori per il controllo della costruzione.
2.1 Prescrizioni per il produttore di calcestruzzo
-
- Obbligo della certificazione del calcestruzzo industrializzato richiesta dal DM del 17 gennaio 2018 (1) in accordo alle Linee Guida Ministeriali sul calcestruzzo preconfezionato (7).
- Tipo di struttura: C.A.
- Provini: cubici.
- Resistenza caratteristica: Rck = 40 MPa.
- Tipo di controllo:
- s = 4 MPa .
- k ● s = 6
- Resistenza a compressione richiesta a 7 giorni ed alla temperatura di 17-23 °C = 30 MPa.
- Classe di consistenza al getto: S5 è slump = 22-24 cm.
- Classe di contenuto in cloruro = 0,20.
- Impermeabilità’: penetrazione dell’acqua minore di 20 mm (secondo UNI EN 12390/8).
- Classe di esposizione: XA1.
- Cemento :CEM III/B 32.5 R.
- Aggregato: Dmax = 25 mm.
2.2 Prescrizioni per l’impresa
- Adottare distanziatori conformi alla realizzazione di un copriferro (cmin,dur) con spessore di almeno 45 mm, in accordo all’Eurocodice 2 con riferimento alla classe di esposizione (XA1), al tipo di struttura (armata) ed alla durabilità dell’opera ( ≥ 100 anni). Garantire, oltre al cmin,dur, anche il valore aggiuntivo di sicurezza (Δcdev) prescritto dal progettista da scegliere tra 10 mm, 5 mm e 0 mm in base all’accuratezza della predisposizione e verifica dei sistemi di distanziatori che egli ha ipotizzato poter essere adottata. Per esempio, se il valore di Δcdev è eguale a 5 mm, il valore del copriferro nominale (cnom)che deve essere specificato sui disegni di progetto diventa: cnom = cmin,dur+ Δcdev = 50 mm.
- Compattare il calcestruzzo in modo che il grado di compattazione del calcestruzzo in opera sia almeno eguale a 0,97.
- Mettere in opera il calcesttruzzo in modo che la resistenza caratteristica del calcestruzzo in sito (Rckis) sia almeno eguale a 34 N/mm2 a cioè all’ 85% della resistenza caratteristica di progetto (Rck).
- Stagionare a umido la superficie del calcestruzzo per ≥7 giorni dal getto.
2.3 Raccomandazioni per il Direttore dei Lavori
- Verificare che esista la certificazione del calcestruzzo industrializzato richiesta obbligatoriamente dalle Norme Tecniche per le Costruzioni emanate con il DM del 17 gennaio 2018 (1,7).
- Far prelevare, in sua presenza (o in presenza di un suo tecnico di fiducia esplicitamente delegato), il calcestruzzo fornito per la confezione dei provini da inviare a un Laboratorio Ufficiale con richiesta scritta di eseguire il controllo di accettazione, di tipo A oppure di tipo B, richiesto obbligatoriamente dalle Norme Tecniche per le Costruzioni emanate con il DM del 17 gennaio 2018 (1).
- Se esplicitamente prescritto come controllo aggiuntivo dal progettista oppure nel caso di dubbi sulla messa in opera e/o stagionatura del calcestruzzo o nel caso di risultati non conformi dei controlli di accettazione, accertare, in conformità al parag. 11.2.6 delle Norme Tecniche per le Costruzioni 2018 e alle indicazioni aggiuntive della Circolare esplicativa alle NTC del 19/01/2019 (2), che la resistenza caratteristica della struttura in situ (Rckis), determinata con prove distruttive (carote estratte dalla struttura) o non-distruttive (sclerometria, velocità degli ultrasuoni, ecc) e calcolata secondo le formule indicate nelle LL.GG ministeriali 2017 per la valutazione delle caratteristiche del calcestruzzo in opera (8) o della UNI EN 13791 (9), sia almeno eguale a 34 MPa e cioè al 85% della resistenza di progetto (Rck); comunicare al progettista di procedere alla verifica della sicurezza della struttura qualora questo requisito non sia soddisfatto.
- Misurare con prove distruttive o non-distruttive (magnetometria) lo spessore del copriferro per verificare che esso sia almeno eguale a quello precisato nel progetto (50) e comunicare al progettista di verificare la sicurezza e la durabilità dell’opera qualora questo requisito non sia rispettato.
- Determinare il grado di compattazione gc mediante l’equazione gc = mv / mv0 (dove mv e mv0 sono rispettivamente il valore medio della massa volumica delle carote estratte dalla struttura dopo almeno 1 giorno dal getto e di quella dei provini prelevati durante il controllo di accettazione) e sia verificato che gc sia almeno eguale a 0,97.
Seconda parte: il grattacielo
Fig.28- il nome dell’opera è Il Grattacielo di Roma
Fig.29-Il nome della struttura è Il grattacielo
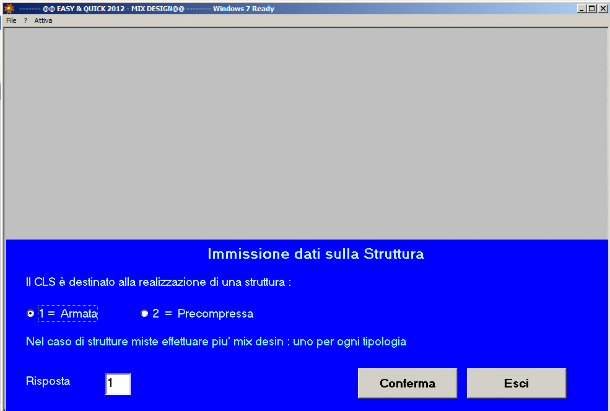
Fig. 30 – La struttura è armata
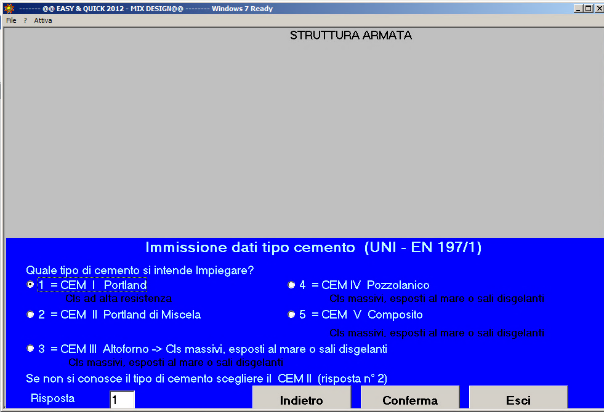
Fig. 31- Si impiega il cemento Portland CEM I
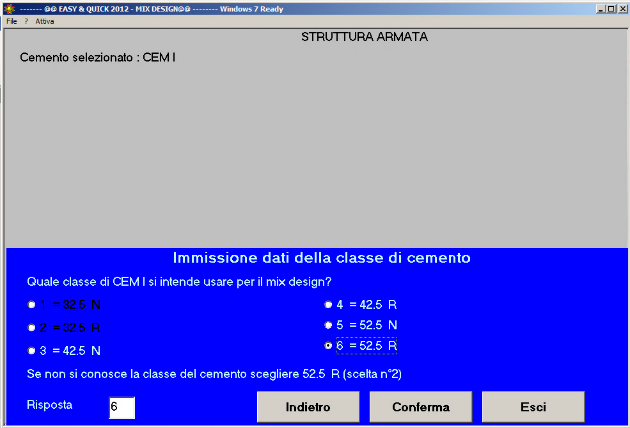
Fig. 32 – La classe di resistenza del cemento è 52.5 R
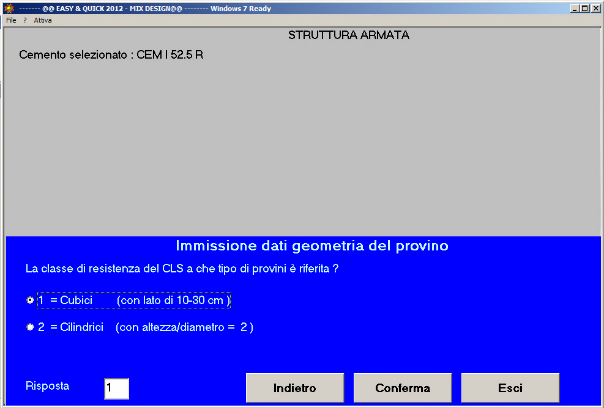
Fig. 33 – I provini sono cubici
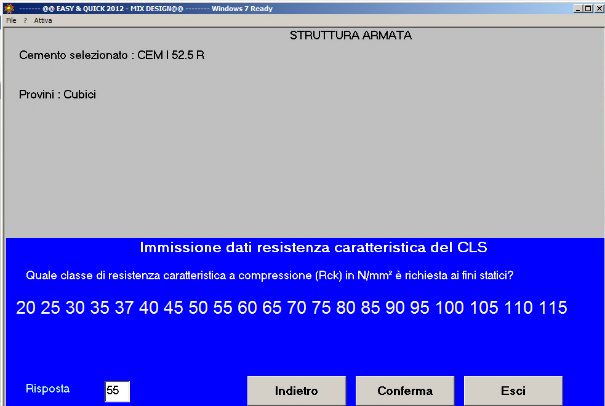
Fig. 34 – La resistenza caratteristica del calcestruzzo è 55 N/mm2
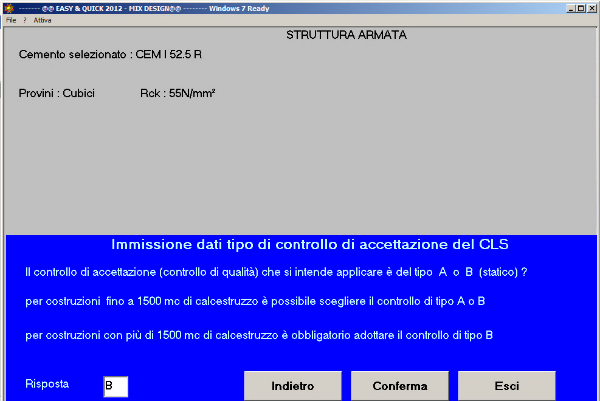
Fig. 35- Il tipo di controllo di accettazione del calcestruzzo è B
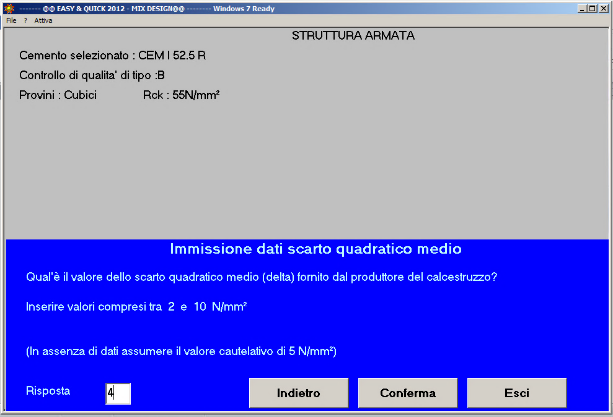
Fig. 36 – Lo scarto quadratico medio è 4 N/mm2
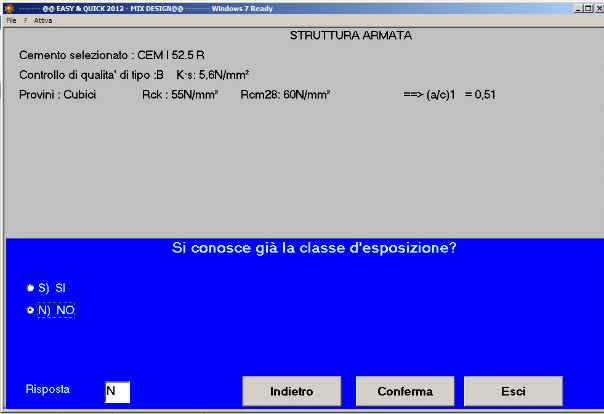
Fig. 37- Non si conosce la classe di esposizione
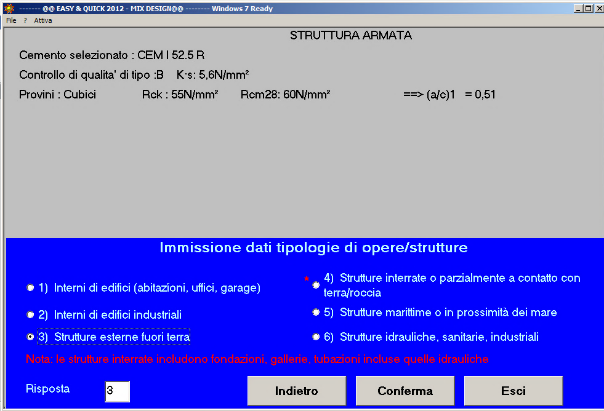
Fig. 38 – La struttura è esterna fuori terra
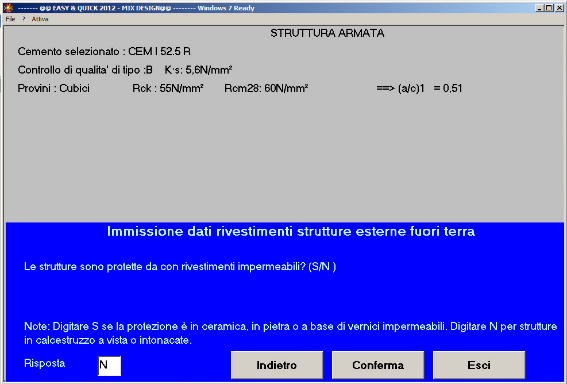
Fig. 39 – La struttura non è protetta con rivestimenti impermeabili
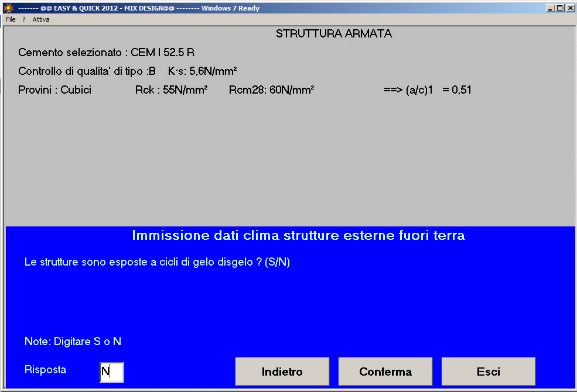
Fig. 40- La struttura non è esposta a cicli di gelo-disgelo
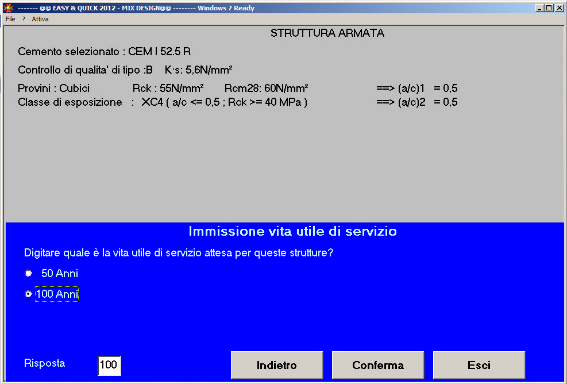
Fig. 41- Si richiede una vita utile di servizio di 100 anni
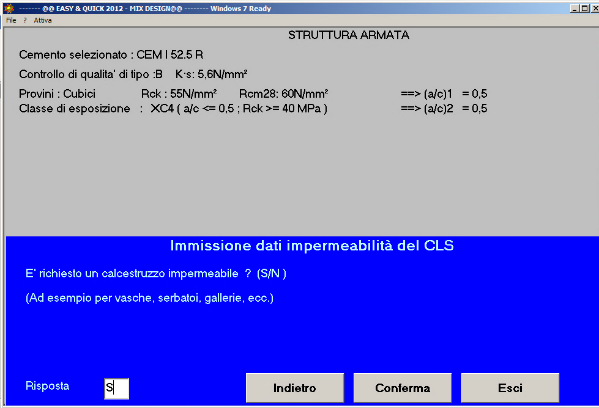
Fig. 42- Si richiede un calcestruzzo impermeabile
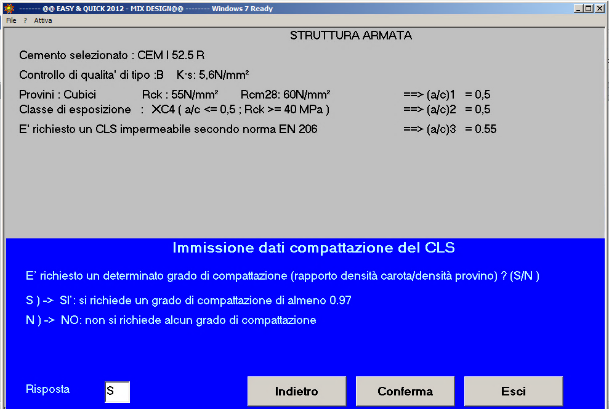
Fig. 43- Si richiede un grado di compattazione di 0,97
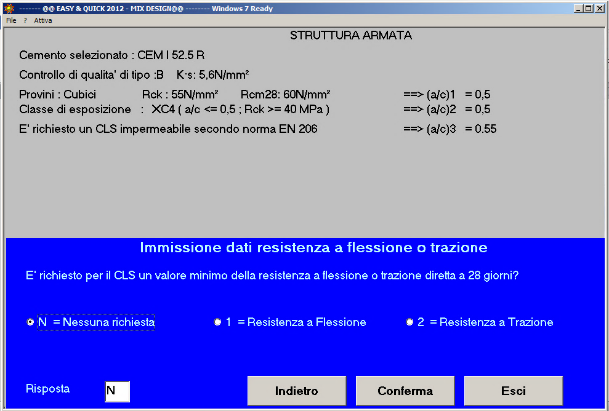
Fig. 44- Non si richiede una resistenza a flessione o a trazione
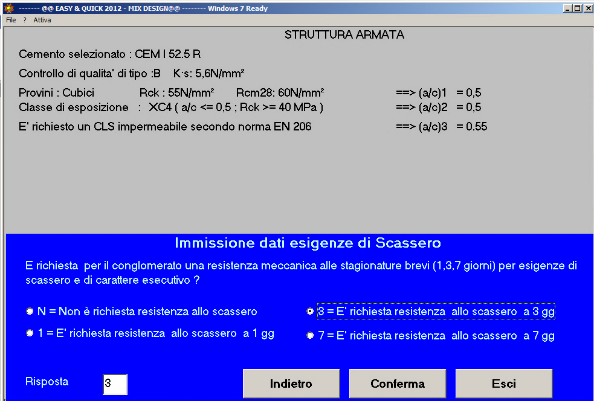
Fig. 45 – Si richiede una resistenza meccanica allo scassero a 3 giorni
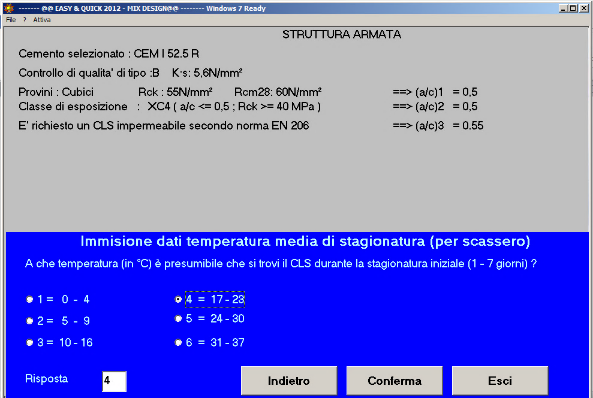
Fig. 46 – La temperatura presumibile durante i primi 3 giorni è 17-23 °C
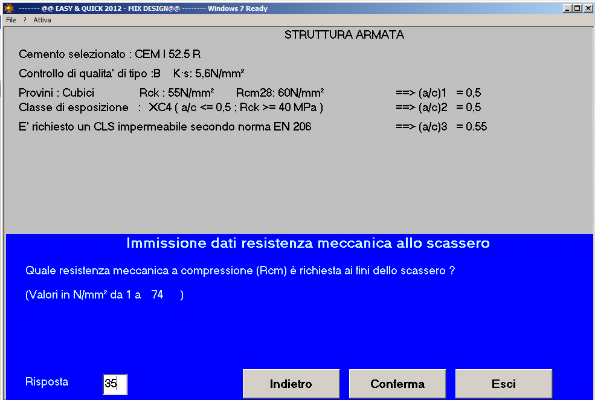
Fig. 47-La resistenza meccanica a compressione richiesta allo scassero è di 35 N/mm2
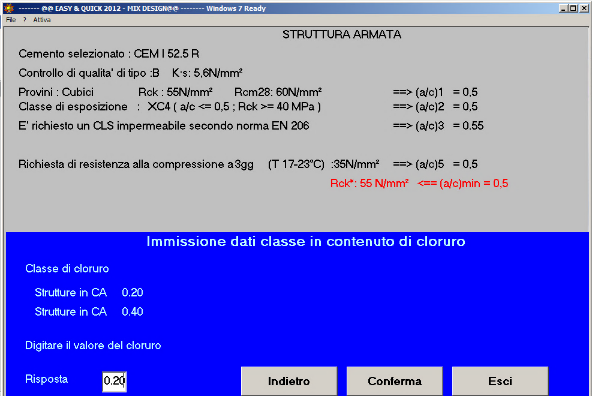
Fig. 48- La classe di contenuto in cloruro è 0,20
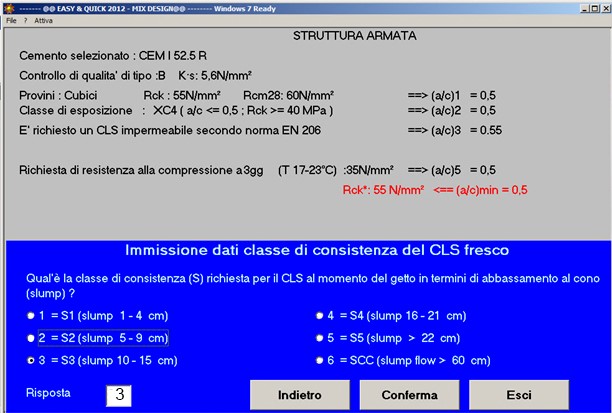
Fig. 49-La classe di consistenza del calcestruzzo fresco è S3
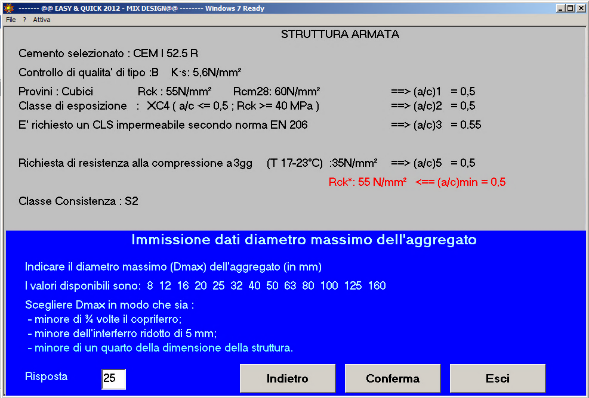
Fig. 50-Il diametro massimo dell’aggregato è 25 mm
3 Prescrizioni da inserire in capitolato per il calcestruzzo del Grattacielo
Adottando lo stesso metodo impiegato per emanare le prescrizioni della fondazione si arriva alle prescrizioni per il Grattacielo comprendente pilastri, pavimenti e muri dei vari piani, con una durabilità di almeno 100 anni.
3.1 Prescrizioni per il produttore di calcestruzzo
-
- Obbligo della certificazione del calcestruzzo industrializzato richiesta dal DM del 17 gennaio 2018 (1) in accordo alle Linee Guida Ministeriali sul calcestruzzo preconfezionato (7).
- Tipo di struttura: C.A.
- Provini: cubici.
- Resistenza caratteristica: Rck = 55 MPa.
- Tipo di controllo: B.
- s = 4 MPa.
- k ● s = 6 MPa.
- Resistenza a compressione richiesta a 3 giorni ed alla temperatura di 17-23 °C = 30 MPa.
- Classe di consistenza al getto: S3 è slump = 100-150 mm.
- Classe di contenuto in cloruro: 0,20.
- Impermeabilità’: penetrazione d’acqua minore di 20 mm (secondo UNI EN 12390/8).
- Classe di esposizione: XC4.
- Cemento: CEM I 52.5 R.
- Aggregato: Dmax = 25 mm.
3.2 Prescrizioni per l’impresa
-
- Adottare distanziatori conformi alla realizzazione di un copriferro con spessore di almeno 40 mm, in accordo all’Eurocodice 2 con riferimento alla classe di esposizione (XC4), al tipo di struttura (armata) ed alla durabilità dell’opera (almeno 100 anni). Garantire, oltre al cmin,dur, anche il valore aggiuntivo di sicurezza (Δcdev) prescritto dal progettista da scegliere tra 10 mm, 5 mm e 0 mm in base all’accuratezza della predisposizione e verifica dei sistemi di distanziatori che egli ha ipotizzato poter essere adottata. Se per esempio Δcdev è pari a 5 mm il valore del copriferro nominale (cnom) che deve essere specificato sui disegni diventa: cnom= cmin,dur + Δcdev = 45 mm.
- Compattare il calcestruzzo in modo che il grado di compattazione del calcestruzzo in opera sia almeno eguale a 0,97, cioè che la massa volumica della carota estratta dalla struttura anche ad 1 giorno dal getto sia almeno pari a 97% della massa volumica del calcestruzzo compattato a rifiuto dei provini cubici o cilindrici sui quali misurare la resistenza caratteristica.
- Mettere in opera il calcestruzzo in modo che la resistenza caratteristica in sito (Rckis) sia almeno eguale a 48 N/mm2, cioè all’ 85% della resistenza caratteristica di progetto Rck.
- Stagionare ad umido le superfici del calcestruzzo per almeno 3 giorni dal getto proteggendole con teli di plastica.
- Rimuovere i teli di plastica.
- Inserire una barriera anti-radon tra la fondazione e il pavimento del primo piano risvoltando il materiale anti-radon nei muri a contatto con il pavimento ed incollare questo materiale con un adesivo indicato dal produttore del materiale.
- Coprire il materiale anti-radon con un foglio di tessuto-non tessuto o di polietilene per proteggere il materiale anti-radon dalle successive operazioni.
- Posizionare i ferri di armatura in modo che lo spessore di copriferro superiore sia almeno 45 mm.
- Gettare il calcestruzzo e spianarlo.
- Costipare il calcestruzzo con un grado di compattazione di almeno 0,97.
- Applicare in superficie lo spolvero indurente appena il pavimento è pedonabile ed incorporarlo mediante pale rotanti.
- Stagionare a umido il calcestruzzo per almeno 3 giorni con teli impermeabili.
- Eseguire sul pavimento i giunti di contrazione.
- Chiedere all’ufficio dell’ARPA (Associazione Regionale per Protezione dell’Ambiente) di misurare e certificare la radioattività nell’edificio che deve risultare inferiore a 300 Bq/m3 o a 200 Bq/m3 rispettivamente per le costruzioni erette prima o dopo il 31 dicembre 2024.
3.3 Raccomandazioni per il Direttore dei Lavori
-
- Verificare che esista la certificazione del calcestruzzo industrializzato richiesta obbligatoriamente dalle Norme Tecniche per le Costruzioni emanate con il DM del 17 gennaio 2018 (1,7).
- Chiedere all’Ufficio dell’ARPA se la misura certificata della radioattività nella costruzione del primo piano sia inferiore a quella ritenuta pericolosa.
- Far prelevare, in sua presenza (o in presenza di un suo tecnico di fiducia esplicitamente delegato), il calcestruzzo fornito per la confezione dei provini da inviare a un Laboratorio Ufficiale con richiesta scritta di eseguire il controllo di accettazione, di tipo A oppure B, richiesto obbligatoriamente dalle Norme Tecniche per le Costruzioni emanate con il DM del 17 gennaio 2018 (1).
- Determinare il grado di compattazione (gc) mediante l’equazione gc = mv / mv0 (dove mv e mv0 sono rispettivamente il valore medio della massa volumica delle carote estratte dalla struttura dopo almeno 1 giorno dal getto e di quella dei provini prelevati durante il controllo di accettazione) e sia verificato che gc sia almeno eguale a 0,97.
- Se esplicitamente prescritto come controllo aggiuntivo dal progettista oppure nel caso di dubbi sulla messa in opera e/o stagionatura del calcestruzzo o nel caso di risultati non conformi dei controlli di accettazione, accertare, in conformità alle Norme Tecniche per le Costruzioni 2018 (1), e alle indicazioni aggiuntive della Circolare esplicativa alle NTC del 19/01/2019 (2), che la resistenza caratteristica della struttura in opera (Rckis), determinata con prove distruttive (carote estratte dalla struttura) o non-distruttive (sclerometria, velocità degli ultrasuoni, ecc), e calcolata secondo le formule indicate nelle LL.GG ministeriali 2017 per la valutazione delle caratteristiche del calcestruzzo in opera (8) o della UNI EN 13791 (9), sia almeno eguale a 47 MPa e cioè all’ 85% della resistenza caratteristica di progetto Rck; comunicare al progettista di procedere alla verifica della sicurezza della struttura qualora questo requisito non sia soddisfatto.
- Misurare con prove distruttive o non-distruttive (magnetometria) lo spessore del copriferro per verificare che esso sia almeno eguale a quello precisato nel progetto (45 mm) e comunicare al progettista di verificare la sicurezza e la durabilità dell’opera qualora questo requisito non sia rispettato.
.
-
Conclusioni
Il programma adottato per emanare le prescrizioni del progettista deve essere completato dalla inserzione di una barriera anti-radon se il pavimento del primo appartamento è in contatto con la fondazione. Occorre inserire una barriera anti-radon tra la fondazione e il pavimento del primo piano risvoltando il materiale anti-radon nei muri a contatto con il pavimento ed incollare questo materiale con un adesivo indicato dal produttore del materiale: entrambe le misure sono state adottate.
Il calcestruzzo deve raggiungere una resistenza a compressione di almeno 30 MPa per sopportare la sollecitazione derivante dal peso del piano soprastante. Ciò comporta che ogni piano sarà gettato su quello precedente dopo 3 giorni.
Le carote estratte dalle strutture per la determinazione della Rckis debbono essere trasformate in cilindri con un rapporto altezza/diametro eguale a 1 per essere comparate con i provini cubici.
Nel caso del getto del calcestruzzo del primo piano è necessario che avvenga dopo 7 giorni dal getto della fondazione quando questa ha raggiunto una resistenza a compressione di 30 MPa.
Le principali differenze tra le prescrizioni per la fondazione e quelle per il grattacielo sono:
- la classe di consistenza al getto: S3 per il grattacielo e S5 per la fondazione; la scelta di S3 per il grattacielo consente, dopo aver compattato a rifiuto il calcestruzzo fresco, di far indurire rapidamente il calcestruzzo e di poter sorreggere a 3 giorni il calcestruzzo fresco del piano superiore;
- la resistenza caratteristica Rck è 55 MPa per il grattacielo contro 40 MPa per la fondazione;
- la resistenza meccanica a compressione di 30 MPa è raggiunta a 3 gg per il grattacielo e a 7 giorni per la fondazione;
- la classe di cemento: CEM I 52.5 R per il grattacielo contro CEM III/B 32.5 R per la fondazione;
- il copriferro nominale (cnom) è pari a 50 mm per le strutture in C.A. della fondazione e 45 mm per le strutture in C.A. del grattacielo.
BIBLIOGRAFIA
-
- Norme Tecniche per le costruzioni (NTC) DM 17/01/2018
- Circolare esplicativa alle NTC, N.7 del 21/01/2019
- UNI EN 197/1:2011 – Cemento – Parte 1: Composizione, specificazioni e criteri di conformità per cementi comuni
- UNI EN 206:2016 – Calcestruzzo – Specificazione, prestazione, produzione e conformità
- UNI EN 1992-1-1: Eurocodice 2 – Progettazione delle strutture di calcestruzzo – Parte 1-1: Regole generali e regole per gli edifici
- MARIO COLLEPARDI, SILVIA COLLEPARDI, ROBERTO TROLI, “Il Nuovo Calcestruzzo”, Settima Edizione, Edizioni TREVISOSTAMPA, pp. 201-220, (2022).
- Linee Guida Servizio Tecnico Centrale Consiglio Superiore. dei LL.PP. per la produzione, il trasporto ed il controllo del calcestruzzo preconfezionato (2008)
- Linee Guida Servizio Tecnico Centrale Consiglio Superiore dei LL.PP. per La valutazione delle caratteristiche del calcestruzzo in opera – Settembre 2017
- UNI EN 13791 – Valutazione della resistenza a compressione in sito nelle strutture e nei componenti prefabbricati di calcestruzzo
INFORMAZIONI SUGLI AUTORI DEGLI ARTICOLI
Mario Collepardi si è laureato in Chimica Industriale con il massimo dei voti nell’Università La Sapienza di Roma. Nel 2007 ad Atlanta (USA) è stato nominato Honorary Member of the American Concrete Institute. Nel 2017 a Bergamo è stato nominato Socio Onorario dell’AICAP. Dal 1969 al 2004 ha insegnato Scienza e Tecnologia dei Materiali nelle Facoltà di Ingegneria delle Università di Cagliari, di Roma La Sapienza, di Ancona oltre che al Politecnico di Milano. È autore di oltre pubblicazioni e di una decina di libri sul calcestruzzo pubblicati in italiano, inglese, cinese e ceco. Nel 1997 a Roma il Consiglio delle Ricerche del Canada e l’American Concrete Institute hanno organizzato in suo onore il “MARIO COLLEPARDI SYMPOSIUM”.
Silvia Collepardi si è laureata a Padova in Ingegneria Civile ed è Amministratore della EN.CO di Villorba (TV) dove è anche direttrice del Laboratorio Ufficiale per le prove sui materiali da Costruzione. È autrice di numerosi articoli e di alcuni libri sul calcestruzzo pubblicati in italiano, inglese e cinese. Nel 2015 ad Ottawa (Canada) Silvia Collepardi ha ricevuto l’Award dall’American Concrete Institute per i “significativi e costanti contributi nella vasta area della tecnologia del calcestruzzo e per la certificazione dei materiali per il loro impiego nel calcestruzzo”.
Roberto Troli si è laureato ad Ancona in Ingegneria Civile con il massimo dei voti e lode. Roberto Troli ha lavorato nella EN.CO come Direttore Tecnico per la messa a punto di nuovi calcestruzzi e per l’assistenza tecnica in contestazioni legali. È autore di numerosi articoli e di alcuni libri sul calcestruzzo pubblicati in italiano, inglese e cinese. Nel 2009 a Siviglia (Sagna) ha ricevuto l’Award dall’American Concrete Institute per i suoi “notevoli contributi alla fondamentale conoscenza dei superfluidificanti ed al loro impiego nel calcestruzzo”. Dal 2021 Roberto Troli è Direttore Tecnologico della Betonrossi di Piacenza.
Deformazione viscosa del calcestruzzo
La viscosità (o la deformazione viscosa o anche creep in inglese) rappresenta la variazione unitaria di lunghezza quando il calcestruzzo indurito è sottoposto all’azione di una sollecitazione di compressione o di trazione permanente per un determinato tempo, di solito continuamente, più raramente variabile ciclicamente.
Il professor Mario Collepardi ce ne parla nell’appuntamento di didattica online di oggi, in cui vedremo:
- le definizioni di deformazione viscosa (creep) e rilassamento;
- il creep puro e da essiccamento;
- la correlazione del creep con la deformazione elastica e con il ritiro igrometrico;
- i parametri che influenzano il creep;
- esempi numerici per calcolare il creep.
Riguarda il video della conferenza sul “Introduction to concrete terminology”
Anche le persone di madre lingua Inglese come un britannico o un nord-americano non sono in grado di comprendere gli argomenti che riguardano la tecnologia del calcestruzzo scritti o parlati in Inglese, a meno che non siano persone esperte in calcestruzzo. Per questo motivo la Enco ha pubblicato il libro in Inglese THE NEW CONCRETE del quale in allegato sono riportati i giudizi molto positivi espressi da scienziati e tecnologhi di fama internazionale che lavorano o hanno lavorato in USA, Canada, Russia, Regno Unito, Francia, Germania, Italia, Cina e Giappone. Inoltre sono anche disponibili sul sito www.encosrl.it due corsi di formazione telematica in lingua inglese intitolati CONCRETE TECHNOLGY: BASIC PRICIPLES e SPECIAL CONCRETES, dove le scritte in Inglese che appaiono sullo schermo sono accompagnate da un commento orale in lingua Inglese, cosicché i partecipanti alla videoconferenza imparinp a pronunciare correttamente i termini Inglesi.
Per avere un’idea su queste iniziative potete riguardare la prima delle due videoconferenze WEBINAR gratuite in lingua Inglese organizzate da ENCO: INTODUCTION TO CONCRETE TERMINOLOGY.
Gli argomenti trattati nella prima videoconferenza INTRODUCTION TO CONCRETE TERMINOLOGY sono:
- gli ingredienti del calcestruzzo;
- le proprietà del calcestruzzo fresco;
- le proprietà del calcestruzzo indurito;
- il comportamento del calcestruzzo ordinario, armato e precompresso;
- la corrosione dei ferri di armatura.
Gli argomenti che verranno trattati nella seconda videoconferenza HIGH STRENGTH CONCRETE venerdì 26 giugno sono:
- i fattori che influenzano la resistenza meccanica;
- impiego combinato di additivi superfluidificanti e fumo di silice;
- il calcestruzzo densificato con piccole particelle (DSP è Densified Small Particles);
- il calcestruzzo a polvere reattiva (RPC è Reactive Powder Concret
- esempi di costruzioni realizzate con calcestruzzo ad alta resistenza meccanica.
Gli argomenti trattati nelle due video-conferenze sono approfonditi nella seconda edizione del libro THE NEW CONCRETE: esso è disponibile per i partecipanti alle videoconferenze WEBINAR al prezzo scontato del 50% incluso il costo di trasporto gratuito in ufficio o domicilio (purché in Italia) facendone richiesta all’indirizzo info@encosrl.it con una mail avente per oggetto “videoconferenze”: sul sito nella sezione LIBRI E FORMAZIONE si possono leggere i titoli dei paragrafi di questo libro.
In alternativa, e preferibilmente, si raccomanda di seguire i corsi telematici CONCRETE TECHNOLOGY: BASIC PRINCIPLES e SPECIAL CONCRETES disponibili sul sito info@encosrl.it nella sezione LIBRI E FORMAZIONE. L’iscrizione a questi corsi è disponibile ai partecipanti alle videoconferenze WEBINAR al prezzo scontato del 50% facendone richiesta all’indirizzo info@encosrl.it con una mail avente per oggetto “videoconferenze”.
Al termine di questi due corsi si può chiedere di sostenere un esame per via telematica per ottenere il Diploma di CONCRETE TECHNOLOGIST firmato dal Direttore dei corsi Prof. Mario Collepardi.
Riguarda il video della conferenza sul “Calcestruzzo a ritiro compensato”
Venerdì 22 maggio si è tenuto, sulla pagina Facebook di Enco Srl, il webinar gratuito “Calcestruzzo a ritiro compensato”. Il calcestruzzo a ritiro compensato è un calcestruzzo speciale per il quale, nel video, vengono descritti i vari metodi per ridurre il ritiro igrometrico, che si manifesta in ambienti con UR inferiore al 95%, e che può provocare fessure sulla superficie del calcestruzzo aggravando la corrosione dei ferri di armatura.
Il metodo più adottato prevede l’impiego di agenti espansivi capaci di provocare un aumento di volume, che compensa il ritiro igrometrico, purché stagionati ad umido per alcuni giorni (da 2 a 7 giorni a seconda dell’agente espansivo). Gli agenti espansivi disponibili sono: CaO, MgO ed 4CaO.3Al2O3.SO3. Nella video-presentazione viene illustrato soprattutto l’impiego del CaO cotto ad alte temperature ed impiegato in combinazione con l’additivo riduttore di ritiro (SRA, acronimo di Shrinkage-Reducing Admixture) capace di enfatizzare le caratteristiche espansive del CaO anche in assenza di stagionatura umida.
Nella conferenza vengono illustrate inoltre alcune interessanti applicazioni del calcestruzzo a ritiro compensato quali:
- la produzione di pavimenti industriali in assenza di giunti di contrazione,
- la produzione di muri alti, curvi, inclinati e lunghi fino a 100 m senza giunti di contrazione come quelli del muso MAXXI di Roma
- il restauro delle strutture in C.A. degradate.
Gli argomenti trattati in questa videoconferenza sono disponibili nella sesta edizione del libro “IL NUOVO CALCESTRUZZO” (autori: Mario Collepardi, Silvia Collepardi e Roberto Troli), disponibile per i partecipanti al WEBINAR al prezzo scontato di 39 € incluso il costo di trasporto gratuito in ufficio o domicilio.
Nella sezione LIBRI E FORMAZIONE del sito si possono leggere i titoli dei paragrafi di questo libro. In alternativa si possono seguire i corsi telematici “TECNOLOGIA DEL CALCESTRUZZO” e “STRUTTURE IN CALCESTRUZZI SPECIALI” disponibili sul sito, sempre nella sezione LIBRI E FORMAZIONE.
L’iscrizione a questi corsi è disponibile ai partecipanti al WEBINAR al prezzo scontato del 50%: sul sito si possono leggere gli argomenti delle lezioni di questi corsi (che rimangono a disposizione dei richiedenti per 40 giorni) ed ascoltare gratuitamente una lezione a titolo di esempio.
Al termine di questi due corsi si può chiedere di sostenere un esame per via telematica per ottenere il certificato di TECNICO DEL CALCESTRUZZO firmato dal Direttore dei corsi Prof. Mario Collepardi.
Riguarda il video della conferenza sulle “Proprietà meccaniche del calcestruzzo”
Venerdì 15 maggio si è tenuto, sulla pagina Facebook di Enco Srl, il webinar gratuito “Proprietà meccaniche del calcestruzzo”. Una videoconferenza dedicata a progettisti, produttori di calcestruzzo, imprese e direttori dei lavori.
Gli obiettivi e le tematiche sviscerati dl professor Mario Collepardi in questo appuntamento sono stati i seguenti:
- Prelievo dei provini per la misura della resistenza meccanica
- Resistenza meccanica a compressione del calcestruzzo
- Resistenza caratteristica
- Resistenza a flessione e a trazione del calcestruzzo
- Comportamento del calcestruzzo ordinario ed armato
Grazie a questo video potete riguardare la conferenza in qualsiasi momento per fare tesoro delle preziose nozioni che il professor Collepardi spiega in maniera chiara e puntuale.
Gli argomenti trattati in questa videoconferenza sono disponibili nella sesta edizione del libro “IL NUOVO CALCESTRUZZO” (autori: Mario Collepardi, Silvia Collepardi e Roberto Troli), disponibile per i partecipanti al WEBINAR al prezzo scontato di 39 € incluso il costo di trasporto gratuito in ufficio o domicilio. Nella sezione LIBRI E FORMAZIONE del sito si possono leggere i titoli dei paragrafi di questo libro.
In alternativa si possono seguire i corsi telematici “TECNOLOGIA DEL CALCESTRUZZO” e “STRUTTURE IN CALCESTRUZZI SPECIALI” disponibili sul sito, sempre nella sezione LIBRI E FORMAZIONE.
L’iscrizione a questi corsi è disponibile ai partecipanti al WEBINAR al prezzo scontato del 50%: sul sito si possono leggere gli argomenti delle lezioni di questi corsi (che rimangono a disposizione dei richiedenti per 40 giorni) ed ascoltare gratuitamente una lezione a titolo di esempio.
Al termine di questi due corsi si può chiedere di sostenere un esame per via telematica per ottenere il certificato di TECNICO DEL CALCESTRUZZO firmato dal Direttore dei corsi Prof. Mario Collepardi.
Non perdere la prossima conferenza su Facebook!

Dizionario enciclopedico del calcestruzzo – Capitolo 19 (parte 2)
Raccolta dei dati storici
La raccolta di tutti i dati sulla “storia” della struttura – dal periodo della costruzione fino alla manifestazione dei segni di degrado – unitamente agli elementi raccolti attraverso il sopralluogo dall’esame visivo, può essere molto utile all’individuazione delle possibili cause di degrado,
i cui riscontri potranno essere trovati attraverso poche ma ben mirate prove in situ sulla struttura o di laboratorio nel seguito discusse.
I dati “storici”, come si può vedere nella Tabella che segue includono quelli relativi al periodo della costruzione, ai materiali impiegati, all’apparizione dei primi segni di degrado, alle condizioni climatiche e di esercizio, ecc.
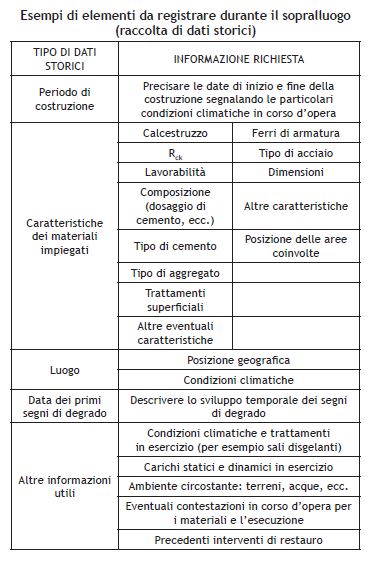
E’ molto importante che i dati “storici” raccolti siano confermati da riscontri oggettivi attraverso le prove, perché molto spesso i dati raccolti a distanza di tempo sono inaffidabili, poco attendibili e quindi talvolta fuorvianti.
Per esempio, il fatto che alcune fessure si siano manifestate dopo alcuni mesi dal getto (←) di una pavimentazione, indica solo che le fessure sono state notate dopo alcuni mesi, ma non esclude che esse si siano innescate, in forma di cavillature poco visibili inizialmente, già dopo poche ore dal getto, come spesso si verifica quando si lavora in climi asciutti e ventilati senza alcuna protezione dall’evaporazione dell’acqua dalle superfici delle pavimentazioni.
Così, anche la manifestazione della corrosione dei ferri viene di solito registrata con l’apparizione delle macchie di ruggine che si formano in superficie dopo alcune piogge, e non già quando appaiono sul copriferro le prime microfessure difficilmente rilevabili a vista. D’altra parte, se le microfessure del copriferro appaiono, per esempio, sull’intradosso di una trave da ponte dopo pochi giorni o mesi di esercizio, è probabile che la microfessurazione abbia un’origine meccanica e che essa sia rapidamente seguita da fenomeni di corrosione dei ferri per la facilitata penetrazione degli agenti aggressivi (aria e umidità) attraverso il copriferro già fessurato.
Se, invece, le fessure appaiono dopo qualche anno è più probabile che la fessurazione sia stata indotta da fenomeni di corrosione dei ferri (promossa dagli stessi agenti aggressivi attraverso un calcestruzzo poroso ma non fessurato). Nei due esempi ora menzionati, quindi, il tempo di apparizione delle fessure può in via ipotetica indicare se le fessure del copriferro siano la causa o l’effetto della corrosione dei ferri. E’ evidente, in questo caso, come un esame dello stato di carbonatazione o di penetrazione dei cloruri all’interno del copriferro (uniforme, oppure differenziato ed accentuato in corrispondenza delle fessure) potrà dare conferma o meno alle ipotesi sopra avanzate. Si può notare, in questo caso, come la raccolta dei dati “storici” e l’esame visivo del degrado, se non sono in grado da soli di portare ad una diagnosi ben definita ed attendibile, consentono tuttavia di limitare a pochi ma ben mirati prelievi da analizzare in laboratorionper l’emissione di una diagnosi.
Prove in situ ed in laboratorio
La raccolta di risultati sperimentali determinati in sito o in laboratorio si basa sull’esecuzione di prove che possono essere suddivise in prove distruttive (←) o semi-distruttive (←) e prove non-distruttive (←).
La distinzione tra prove distruttive e prove non-distruttive consiste fondamentalmente nel fatto che le prime si basano su prove sperimentali, generalmente eseguite in laboratorio, effettuate su provini o campioni prelevati dalla struttura: ne consegue che esse prevedono in genere lo scrostamento di frammenti di intonaco, il sollevamento sia pure parziale di un rivestimento del pavimento, il carotaggio di una muratura, ecc., tutte operazioni che possono arrecare una compromissione, sia pure modesta o trascurabile, a costruzioni quantomeno sospettate di essere coinvolte da un processo di deterioramento. Le prove semi-distruttive provocano un danno più limitato, rispetto alle prove distruttive, e confinato solo allo spessore corticale della struttura.
Le prove non-distruttive, invece, presentano il vantaggio di fornire elementi utili alla interpretazione del potenziale deterioramento in atto, senza minimamente danneggiare lo stato dell’edificio o della struttura dal punto di vista estetico o strutturale. Le prove non-distruttive consistono in misure di carattere prevalentemente fisico o fisico-meccanico, come per esempio la determinazione della durezza superficiale – sclerometria (←) – o della velocità delle onde ultrasoniche (←) da eseguire in sito sulla struttura; le prove distruttive, invece, sono prevalentemente di carattere chimico o chimico-fisico da effettuare in laboratorio. Inoltre, le prove non-distruttive in sito forniscono dei dati soprattutto sul dissesto delle strutture (per esempio: cedimenti di fondazioni, sovraccarichi, ecc.) che non necessariamente coinvolgono il degrado dei materiali. Le prove distruttive effettuate in laboratorio, invece, sono prevalentemente finalizzate alla valutazione del degrado dei materiali (per esempio: distacco parziale di intonaco, rigonfiamento di una muratura, corrosione di un metallo, ecc.) che non necessariamente significano un dissesto strutturale dell’edificio.
In generale, è molto difficile che con le sole prove non-distruttive si possa arrivare ad una diagnosi corretta del degrado di una struttura. Molto spesso, esse devono essere comparate con quelle distruttive. L’accoppiamento di prove distruttive e non-distruttive, oltre al carattere di complementarità e di completezza dell’informazione desunta, presenta anche il vantaggio di ridurre globalmente il numero totale delle prove da eseguire e quindi il costo generale della diagnosi: infatti, in linea di massima, il costo della singola prova di laboratorio è relativamente basso, ma si richiede un numero relativamente elevato di prove sui diversi prelievi, rispetto alle prove non-distruttive, per poter emettere una diagnosi.
Dizionario enciclopedico del calcestruzzo – Capitolo 19 (parte 1)
Diagnosi del degrado delle strutture in calcestruzzo. La diagnosi del deterioramento di un edificio o di una struttura in calcestruzzo si basa sull’esame visivo del degrado e sulla raccolta di dati storici che – unitamente ai risultati di prove eseguite in sito o in laboratorio su
frammenti di materiale prelevati dalla struttura – consentono di stabilire le cause del degrado della struttura in genere, e del deterioramento dei materiali in particolare (M. Collepardi, S. Collepardi, J.J. Ogoumah Olagot, F. Simonelli e R.Troli, “Diagnosi del degrado e restauro
delle strutture in C.A.”, Seconda Edizione Tintoretto, Villorba, TV, 2010). Nella Figura che segue è illustrato schematicamente il processo per arrivare alla emissione di una diagnosi del degrado:
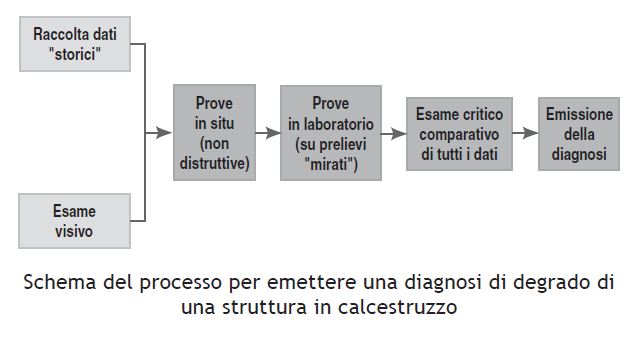
Si può dividere il processo di diagnosi in tre stadi:
– esame visivo del degrado;
– raccolta dei dati storici;
– prove in situ ed in laboratorio.
Esame visivo del degrado
L’esame visivo può fornire utili indicazioni circa la raccolta di alcuni elementi indispensabili alla preliminare individuazione del fenomeno almeno per come esso si manifesta apparentemente. Un’accurata documentazione fotografica dei difetti, localizzati in relazione ad un disegno dell’opera coinvolta dal degrado, può essere molto utile per la preparazione di un dossier finalizzato all’emissione della diagnosi. La Tabella che segue riassume schematicamente alcune di queste indicazioni che, attraverso il sopralluogo, è opportuno raccogliere e documentare
sistematicamente per inquadrare la tipologia del degrado così come esso si manifesta: fessurazioni (←), corrosione dei ferri di armatura (←) scoperti, delaminazioni superficiali o distacchi profondi di calcestruzzo.
Esempi di utili elementi da registrare durante il sopralluogo (esame visivo)
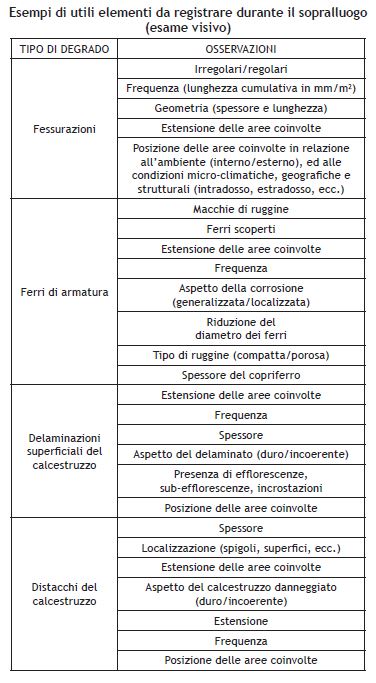
Per esempio, l’apparizione di fessure di forma irregolare e magari localizzate sulle pavimentazioni, ma non sulle strutture casserate (travi, pilastri, ecc.), può essere il sintomo di una fessurazione indotta dal ritiro plastico (←) per assenza di stagionatura umida (←) subito dopo la finitura del pavimento. D’altra parte, la presenza di fessure dislocate quasi regolarmente —per esempio in corrispondenza di determinati ferri di armatura— lungo strutture casserate può segnalare indicativamente l’apparizione di fessure indotte successivamente per effetto del ritiro igrometrico (←) a causa di un’eccessiva quantità di acqua di impasto (←) e/o dosaggio di cemento (←) nel calcestruzzo. Le fessure su una pavimentazione dislocate quasi sistematicamente tra due giunti di contrazione (←) potrebbero far pensare più che al ritiro
plastico ad un eccessivo ritiro igrometrico manifestatosi prima del taglio dei giunti di contrazione eseguito tardivamente.
Analoghe considerazioni possono essere estese alla registrazione della situazione sullo stato dei ferri scoperti oppure alle tipiche macchie di ruggine sulla superficie della struttura. Il numero, l’estensione e la dislocazione dei difetti in relazione alle condizioni geografiche e micro-climatiche, come anche la distribuzione dello spessore dei copriferri eventualmente divelti, sono tutti elementi utili per la sintomatologia del degrado.
Infine, i difetti del calcestruzzo in forma di delaminazioni estese e sottili o di danneggiamenti più profondi in corrispondenza di determinate aree per esempio in spigoli, pareti, zone di bagnasciuga, scarichi pluviali, ecc. presenti nell’intradosso (←) o nell’estradosso (←) sono tutti elementi molto importanti da registrare unitamente allo stato di coesione del materiale danneggiato (duro, fragile, polverulento, molle, ecc.) e di eventuali depositi superficiali (efflorescenze, incrostazioni, ecc.).
Dizionario enciclopedico del calcestruzzo – Capitolo 18
Corrosione promossa dal cloruro. La depassivazione (←) delle armature metalliche, cioè la perdita del carattere protettivo da parte del film di ossido ferrico nei confronti del substrato metallico, può avvenire anche per la presenza dello ione Cl- sulla superficie dei ferri di armatura, a seguito dell’esposizione ai cloruri presenti nei sali disgelanti applicati d’inverno sulle pavimentazioni o nelle acque marine. Anche in questo caso, oltre alla depassivazione provocata dal cloruro, è necessario che il processo di corrosione sia alimentato da ossigeno ed acqua. Per esempio, nelle strutture in C.A. (←) immerse in acqua di mare la corrosione è trascurabile per la bassa concentrazione di ossigeno nell’acqua indispensabile per alimentare il processo corrosivo; nelle strutture semi-immerse, invece, l’alternanza di bagnato-asciutto dovuta al moto ondoso o alle maree, accelera fortemente la corrosione perché sia l’aria con l’ossigeno (nei periodi asciutti) sia l’acqua con i cloruri (nei periodi di bagnatura) possono accedere ai ferri di armatura. Un’analoga situazione di alternanza bagnato-asciutto si verifica nelle strutture armate esposte ai sali disgelanti, ancorché l’esposizione al cloruro sia limitata a qualche mese per anno. A parte la protezione del calcestruzzo dalla penetrazione del cloruro (←) l’impiego di acciaio inossidabile (←) comporta una migliore durabilità (←) delle strutture in C.A. (←) e C.A.P (←).
Corrosione sotto sforzo -> vedi Stress corrosion.
Cosa -> vedi Porto di Cosa.
Creep -> vedi Deformazione viscosa.
Creep fondamentale -> vedi Creep puro.
Creep puro. Deformazione viscosa in assenza di ritiro igrometrico (←). -> vedi Deformazione viscosa.
Cristallino. E’ il reticolo degli atomi o degli ioni che si collegano in forma ordinata formando un cristallo; per esempio il quarzo (←), chimicamente SiO2 possiede un reticolo formato da atomi di silicio ed ossigeno collegati in forma geometricamente regolare; al contrario, nella silice amorfa (←) (anch’essa chimicamente SiO2) gli atomi di Si ed O sono collegati in forma disordinata -> vedi Pozzolana dove la Figura illustra la differenza nei reticoli degli atomi tra quarzo cristallino e silice amorfa con attività pozzolanica.
Cristallografia. Scienza basata sulla legge di Bragg (←) per determinare la distanza tra i piani reticolari di un solido cristallino (←) -> vedi Analisi per diffrazione dei raggi X.
Cristobalite. Forma cristallina di SiO2. -> vedi Polimorfismo della silice.
Crivello. Telaio con fondo in lamina perforata. -> vedi Analisi granulometrica.
Cromo. Nel cemento può essere contenuta una certa quantità di cromo in diverse forme note come II (bivalente), III (trivalente), ecc. Il cromo esavalente (VI) deve essere presente in quantità limitata (non superiore a 2 mg/kg) perché cancerogeno. Per questo motivo è necessario aggiungere nel mulino di macinazione del cemento un agente cosiddetto cromo-riducente capace di trasformare il cromo esavalente in forme di cromo di minore valenza e non pericolose. L’agente riducente più utilizzato è il solfato ferroso ancorché esistano altri prodotti cromo-riducenti a base di sali di antimonio e di stagno. Il solfato ferroso viene dosato allo 0,25-0,3% circa e a questi dosaggi non influenza l’idratazione del cemento. Tuttavia, a contatto con l’aria si carbonata perdendo il suo potere riducente nei confronti del cromo esavalente. Pertanto, nel cemento distribuito in sacchi deve essere indicata la data di confezionamento e il periodo di stoccaggio durante il quale il contenuto di cromo esavalente rimane inferiore allo 0,0002% del peso totale del cemento.
Dizionario enciclopedico del calcestruzzo – Capitolo 17
Corrosione promossa dalla carbonatazione. L’aria – ed in particolare l’anidride carbonica, l’ossigeno e l’umidità in essa contenuti – può provocare la corrosione delle armature metalliche a seguito di un fenomeno denominato carbonatazione (←). In realtà, il ruolo dell’anidride carbonica (CO2) è quello di un complice, mentre i veri killer nei confronti dei ferri sono l’ossigeno e l’umidità contenuti nell’aria, come è mostrato nel processo che riguarda la corrosione dei ferri di armatura (←).
Inizialmente nel calcestruzzo si stabiliscono, per lo sviluppo della calce di idrolisi (←), Ca(OH)2, a seguito dell’idratazione del cemento (←), condizioni di forte basicità (pH>13) particolarmente favorevoli alla buona conservazione delle armature metalliche; in queste condizioni, infatti, sul ferro si forma un film di ossido ferrico impermeabile e adesivo al substrato metallico; in questa situazione, detta di passivazione (←), la pellicola impermeabile di ossido ferrico impedisce all’ossigeno ed all’umidità di arrivare al ferro metallico che si trova sotto il film impermeabile e pertanto impedisce la formazione di ruggine secondo lo schema del processo sopra mostrato. Quando però la zona di calcestruzzo che protegge i ferri, il copriferro (←), è completamente penetrata dall’anidride carbonica, la situazione cambia radicalmente. Infatti, l’anidride carbonica annulla la basicità a seguito del processo di carbonatazione che consiste
nella trasformazione della calce di idrolisi in carbonato di calcio (CaCO3):
Ca(OH)2 + CO2 -> CaCO3 + H20
In seguito della carbonatazione, la calce di idrolisi è in tutto o in parte neutralizzata e il pH scende a valori di circa 9: il ferro, già a pH minori di 11, perde la sua passività (depassivazione (←)), cioè è in grado di subire la corrosione secondo la reazione che porta alla formazione di ruggine sopra mostrata. In sostanza, il film di ossido di ferro inizialmente protettivo (per la sua impermeabilità all’ossigeno ed all’acqua) diventa poroso ed incoerente se il pH scende sotto 11 e non è più in grado di bloccare l’accesso dell’ossigeno e dell’umidità al substrato metallico. In queste condizioni, a seguito della trasformazione del ferro in ruggine (circa 6-7 volte più voluminosa del metallo), il copriferro viene prima fessurato e quindi espulso come è mostrato nella Figura che segue:

La carbonatazione, di per sé, non danneggia il calcestruzzo e neppure danneggia direttamente i ferri di armatura. Essa crea solo le condizioni favorevoli al processo di corrosione da parte dell’ossigeno e dell’umidità. In altre parole, un calcestruzzo armato conservato in un ambiente di pura CO2 potrà subire una completa carbonatazione del copriferro senza, però, alcun rischio
di corrosione per le armature metalliche a causa della mancanza dei prodotti (H2O, O2) che alimentano la trasformazione di ferro metallico in ruggine. La velocità con cui il fronte della carbonatazione avanza nel copriferro segue una legge del tipo:
x = K √t
dove x è lo spessore di calcestruzzo penetrato dalla CO2 al tempo t, e K è una costante che dipende dalla qualità del calcestruzzo, in particolare dal rapporto acqua/cemento (←), a/c, oltre che dal tipo e classe di cemento (←), ma anche dall’umidità relativa (UR) dell’aria raggiungendo il valore massimo a circa 60-70% di UR.
Lo spessore carbonatato x è determinabile spruzzando una soluzione di fenolftaleina (←) (il cui colore cambia con il pH, sulla superficie di frattura di un provino di calcestruzzo il quale è rimasto esposto all’aria; lo spessore di calcestruzzo che rimane di colore grigio corrisponde ad x, mentre la parte di calcestruzzo non carbonatata si colora in rosso.







